化学变化中能量变化的主要原因
键能变化
- 物质都有能量,物质的组成、结构、状态不同,所具有的能量也不同。在化学反应中,一定有能量的变化。
- 化学键的断裂和形成需要吸收和释放能量是化学反应中能量变化的主要原因。
- 以
为例:
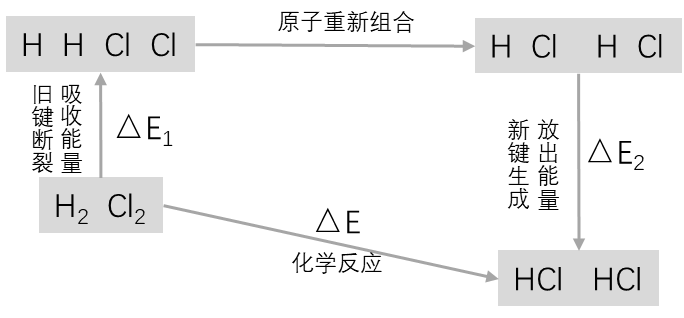
该反应释放的能量 = 生成物中化学键形成所放出的总能量 - 反应物中化学键断裂所吸收的总能量。
如果结果
气体原子结合成每摩尔 放出431KJ 的能量. 每摩 分子断裂成 气体原子, 分别需要吸收436 KJ, 243 KJ 的能量。则每生成2摩 , 反应放热183 KJ 。
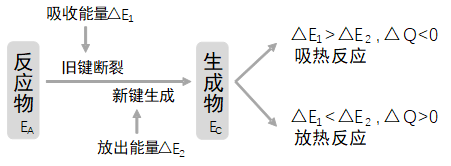
当破坏旧化学键所吸收的能量小于形成新化学键所释放的能量,即
时,则有能量向外界释放,发生放热反应,放出的能量 ; 当破坏旧化学键所吸收的能量大于形成新化学键所释放的能量,即
时,则需从外界吸收能量,发生吸热反应,吸收的能量 。